�����
��������һ����Ϯ��Ƥ��������5��������ֻ��15%-20%���ɺ�ɫ��ϸ����չ���ɡ������ĺ�ɫ��ϸ��ͨ��ճ������E-cadherin��ǻ�ϸ������á��ں�ɫ������չ�����У���ɫ����ϸ��ͨ�����ֻ��ƴӽǻ�ϸ�������ݣ�����E-cadherin�µ���N-cadherin�ϵ������ָ�ճ����ת��ʹ��ɫ����ϸ���ܹ�ֱ������Ƥ�� N-cadherin����ϸ������ã������Щϸ����ת��������Ҫ����Ȼ��ɫ����ϸ������������Ƥϸ���������Ǿ�����һ����������Ƥ�����ת��(EMT)�ı���ת�����̡����磬EMT�յ�����TWIST1��ZEB1�ں�ɫ�������쳣���¼������BRAF�°��������ã��յ���ɫ��ϸ��������ת�����ٽ���ɫ�����ķ�չ��N-cadherin��E-cadherin�������滻�������������ƺ�ɫ����ϸ������ֳ���˶�����Ϯ�������ڽ��������ԡ�ͨ������ԭ����ת���Ժ�ɫ������������IJ��죬��������N-cadherin��E-cadherin��ת�ķ��ӣ���Ϊ��ɫ�����������ṩDZ�ڵ����ưе㡣
Ĥ��������Annexin���Ǹƺ���֬��ϵ���һ�������壬��������ϸ�����̣��������������ź�ͨ·���������ء�ϸ�����Ѻ�ϸ���ֻ���Ĥ������ʧ�������������������ķ�������չ��ء�Annexin A10(ANXA10)��������ֵ�Annexin�����Ա�����ڸΰ������ٰ�����ǻ������Ƥ���ѳ����ȶ����������쳣��������������͵IJ�ͬ��ANXA10�ı�����в�ͬ��Ԥ���ֵ��ANXA10����������ϸ������Ѫ���ַ���������չ��Ԥ�����й�����ǰ���ٰ���θ���Ͱ��װ��У�ANXA10����Ľ�����ϸ����ֳ��Ǩ�Ƶ�����������෴���ڽ�ֱ��������ǻ�۰���ͷ�����۰�����������ת�ƵĻ����У�ANXA10�ı����ϵ���Ԥ������ء���ȻANXA10����ϸ����ֳ���ֻ���ϸ���Ǽ���װ�ĵ��أ�����Ӱ��������չ�Լ�����Ԥ��ķ��ӻ����в������

����

�����
1��ANXA10�ں�ɫ�����б����ϵ������ɫ�����Ľ�չ���
��������ʹ��Oncomine���ݿ������ANXA10�ں�ɫ�����е�mRNA����ˮƽ������������ڰ������Ժ�ɫ����(n=18)��Ƥ����ɫ����(n=45)��Talantov��ɫ����mRNA���ݼ��У�Ƥ����ɫ������ANXA10��mRNA����ˮƽ�����������Ժ�ɫ���롣���߽�����ʹ��TIMER���ݿ������ANXA10�߱���Ժ�ɫ��������������ٴ����塣Kaplan-Meier������ʾ��ANXA10�ĸ߱�����Ƥ����ɫ����(SKCM)���ߵĵ���������أ�������ԭ����Ƥ����ɫ�������ߡ����߽�һ��ͨ�������黯Ⱦɫ����˺�40���˺�ɫ������֯��������֯оƬ��ANXA10�ı�����������ANXA10��ת���Ժ�ɫ�����б��������ϵ��������ɫ�����Ľ�չ��أ���ʾANXA10�����ں�ɫ�����з��������ٽ����á���������������������С���ɫ����ϸ��ϵ��B16F10��B16F1���о�ANXA10�Ĺ��ܣ�B16F10ϸ����B16F1ϸ�����и��ߵ�ת��DZ�ܡ����������ٴ������й۲쵽�Ľ�����ƣ�ANXA10��B16F10ϸ���еı������B16F1ϸ���иߡ�ͬʱ��ANXA10���˺�ɫ����ϸ��ϵA375�еı�����˽����γ�ϸ��HaCaT�еı���ߡ�


2��ANXA10����˺�ɫ������ת������
Ϊ�˽�һ���о�ANXA10�ں�ɫ������չ�е����ã����߽�����ANXA10�ȶ���������ó���B16F10ϸ��ϵ����ϸ����ֳʵ���У���WTϸ����ȣ�ANXA10-KOϸ����ʾ�����Ƶ�ϸ���������ʡ�Ȼ����transwellʵ�������ANXA10�Ĺ����������ٽ�ϸ��Ǩ�ƣ���ANXA10�ı���ȱʧ������������ϸ��Ǩ�ơ����˿�����������Ҳ�۲쵽���ƵĽ�������⣬��ϸ��������ʾ��ANXA10-KOϸ�����ƶ��ٶȱ�WTϸ���������⣬ANXA10�������B16F1ϸ����ϸ��Ǩ����ǿ���� siRNA�鵼��ANXA10�����������Լ��������ķ�ʽ������B16F10ϸ���Ķ���Ǩ�ƣ��Ӷ���һ��֤����ANXA10��ϸ���˶�����Ҫ�ԡ�



�����������������ڼ����ANXA10�ں�ɫ����ת���е����á�������ʵ����һ�£���С���ɫ����ͬ��������ֲ��ģ���У�ANXA10�ı���ȱʧ��Ӱ���ɫ����������������С���ת��ģ�����������ƺ�ɫ������ת�ơ���Ұ����B16F10ϸ����ֲС����ȣ�ANXA10-KOϸ����ֲС��ķ�ת�ƽ���������Լ��٣�����ڴ�С��û�в��졣�ܵ���˵�����ߵĽ���������ں�ɫ�����У�ANXA10��ת���йأ�������ֳ�ء�

3��ANXA10ͨ��TGF-��/SMADͨ·�յ�E-cadherin��N-cadherin��ת��
Ϊ��ȷ��ANXA10�ٽ���ɫ����ת�Ƶķ��ӻ��ƣ����߶�ANXA10-KO���ױ�B16F10ϸ��������ת¼����������ά��ͼչʾ����ANXA10-KO���ױ�B16F10ϸ���ж��м��ص��Ļ���ɽͼչʾ���������������ķֲ���������Pֵ<0.05����SMAD6��SMAD9�Dz�������������Ļ�����ͼ��ʾ���ǵ�ת¼ˮƽ����仯�߶�һ�¡�SMAD6��SMAD9��TGF-��/SMADͨ·�Ĺؼ��������ӣ�KEGGͨ·����Ҳ��������ANXA10-KO��صĻ������仯��TGF-���ź�ͨ·������ء���ɫ����ϸ��ͨ�����ֳ���ת����ɢ��ص�EMT���͡�SMAD������TGF-���ź�ͨ·�ǿ���EMT���ص���Ҫ;��֮һ��TGF-���ź������źż���������SMAD2/3���ữ��SMAD4����λ��TGF-��/SMADӦ������ת¼���Ϊ��֤ʵANXA10�Ƿ����TGF-��/SMAD�źţ��������ANXA10����ȱʧ��TGF-���յ���ϸ�����ź�ת���ı仯��TGF-���յ���SMAD2���ữ��ANXA10-KOϸ���б����ơ�ͬʱ����ANXA10-KOϸ���У�TGF-���յ���SMAD4����λ��TGF-��/SMAD������ת¼������ܵ����ơ�
SMAD6��TGF-��/SMAD�ź�ͨ·�е�������SMAD (I-SMAD)����ANXA10-KO ϸ���У�qRT-PCR��SMAD6��mRNA�����ϵ�������ANXA10�������B16F10ϸ����SMAD6�����µ�����ʾANXA10��SMAD6�и�����ء���Ҫ���ǣ�ANXA10-KOϸ�����ֳ����ߵ�E-cadherin������͵�N-cadherin�������SMAD6�����������Э���ġ���ANXA10-KOϸ���У�����ӫ��ʵ��֤ʵ��N-cadherin��E-cadherin�ı���ת����SMAD6��siRNAs���ſ���ʹE-cadherin��N-cadherin�Ŀ��ػָ�����ˣ�ANXA10����ͨ���µ�TGF-��/SMAD�ź�ͨ·�е�SMAD6���ٽ�E-cadherin��N-cadherin��ת����


4��ANXA10ͨ��PKD1�ź�ͨ·��SMAD6����Ӱ��
��ǰ��һ���о��������ڷγ���άϸ���У�TPA��PKC���Ƽ���ͨ��PKD1ͨ·�µ�SMAD6�ı��PKD1������PKC�̣���һ��PKC��ص�˿����/�հ��ᵰ��ø�����������������B16F10ϸ���ϵ�ʵ�������PKD1�Ĺ������µ���SMAD6�ı����������ANXA10-KOϸ���У�PKD1�������TPA����������ʹ����ȫ������SMAD6�ı������ߡ���Ȥ���ǣ����߷�����ANXA10-KOϸ����PKD1�ı���ˮƽ�����µ�����һ��������ANXA10��siRNA���ŵ�B16F10ϸ���еõ��˽�һ����֤��siRNA���Ŷ�ANXA10�ı�������ѡ���Եؽ�����PKD1�ı���ˮƽ����û�н�������PKC���͵ı���ˮƽ�����һ��յ���SMAD6�����ϵ��Լ�N-cadherin��E-cadherin��ת����������B16F1��B16F10ϸ���н�һ�������ANXA10��PKD1�ı�������ԡ����������PKD1��ANXA10�ʱ�������أ���SMAD6�ʱ��︺��ء���Ұ����B16F10ϸ����ȣ�ANXA10-KOϸ����PKD1�ı���ˮƽ�ϵͣ�SMAD6�ı���ˮƽ��PKD1����ˮƽ�Ľ��Ͷ����ߡ���ˣ�ANXA10��SMAD6�ĸ����ؿ���������PKD1�ź�ͨ·��

5��ANXA10ͨ����PKD1����ö������併��
Ϊ��ȷ��ANXA10��PKD1����ˮƽ�����е����ã��������ȼ����PKD1��ANXA10-KOϸ���е�ת¼����ˮƽ�����������ANXA10�ı���ȱʧ��Ӱ��PKD1��mRNA����ˮƽ��������(CHX)����������PKD1�Ŀ��ٽ��⣬ͬʱ������ANXA10�ı���ˮƽ��MG132��������������PKD1�Ľ��⣬���һָ���ANXA10-KOϸ����PKD1����ˮƽ���½�������ͬʱҲ���֣�ANXA10�Ĺ������Լ��������ķ�ʽ����PKD1�Ķ�۷��ػ���������������ͨ��Co-IPʵ�����ANXA10��PKD1֮�������á���Flag-PKD1��Myc-ANXA10��תȾ��293Tϸ���У�����ͨ��Co-IP���֤ʵ��PKD1��ANXA10֮�������ã���ͨ������ӫ����۲쵽���ǵĹ���λ��Ϊ��ȷ��PKD1��ANXA10����õĽ��������������һϵ��PKD1Ƭ�Ρ�Co-IP������ʾ��Flag-PKD1 (400-551aa��428-748aa)��ANXA10����ã���Щ���ζ�����PKD1(428-550aa)���Ρ�Molecular dockingԤ�������PKD1��ANXA10�Ľ��λ��λ��PKD1�Ħ�����״����(500-550aa)��������λ��PH�ṹ��(400-551aa)�ڣ���PKD1����֮������õı��档���ߵ����ݱ�����ANXA10��һ���µ�PKD1��ص��ף�����PKD1�Ľ��⡣


6��ANXA10����E3����øTRIM41�鵼��PKD1����
����ANXA10��PKD1֮��Ĺ��������߽������о���ANXA10����PKD1����Ļ��ơ�Ϊ���о�PKD1��������B16F10ϸ���еĽ����������磬���߽�Flag-PKD1�������ͨ��anti-Flag����������߳��������PKD1��ظ����������ĵ���ø�к�LC-MS/MS�������е�������ͨ��������������������������Ȥ�ĺ�ѡ���ף�TRIM41��TRIM28�����������ṹ����ij�Ա������E3����ø�Ĺ��ܡ�����ͨ��siRNA����ʹTRIM41��TRIM28�ı����Ĭ��������ANXA10-KOϸ���У�TRIM41��siRNA������ʹPKD1ˮƽ�ָ�����TRIM28��siRNA�������ܡ�ͬʱ��TRIM41�Ĺ����ﵼ��PKD1����ˮƽ�½�������SMAD6����ˮƽ���ߡ����⣬MG132�Ĵ���������TRIM41�����������PKD1����ˮƽ�½�����TRIM41��ΪE3����ø�Ĺ���һ�£���TRIM41������ʱ��PKD1��۷��ػ�ˮƽ���ӣ�˵��TRIM41��PKD1���������E3����ø��
����ͨ��Co-IPʵ��֤����TRIM41��PKD1����ã�����ANXA10������ʱ����������ñ�PKD1��ANXA10���������ȡ���������Ʋ⣬ANXA10����ͨ����PKD1�����������PKD1����TRIM41�鵼�Ľ��⡣Ϊ����֤��һ���裬�����յ�PKD1 (400-551 aa)�ı��ʹ����ΪANXA10-PKD1�������Ƽ�����ANXA10������ϡ�PKD1 (400-551 aa)��������Ч������PKD1����ˮƽ��TRIM41��siRNA���ſ�ʹPKD1����ˮƽ�ָ�����ANXA10ȱʧ��Ч�����ƣ�PKD1 (400-551 aa)�����ﵼ��B16F10ϸ����SMAD6ˮƽ���ߣ�ϸ��Ǩ�Ƽ��١����⣬PKD1 (400-551 aa)�����ﲿ��������TPA�յ���PKD1���ԣ�������ANXA10����ȱʧ��Ч������Щ���������ANXA10ͨ����PKD1��ϲ�����������TRIM41�鵼�ķ��ػ����ö��ϵ�PKD1�ĵ���ˮƽ��

7��ANXA10ͨ��PKD1-SMAD6ͨ·���ٽ�ת��DZ��
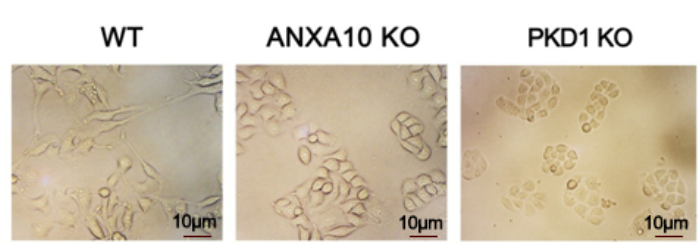
B16F10��һ����ת���Ժ�ɫ����ϸ��ϵ��ϸ���ʵ��͵������ļ��������״��Ȼ�������߹۲쵽��ANXA10-KO��PKD1-KOϸ���У�ϸ����״����ϸ���ķĴ���ת��Ϊ��Բ�Ρ�ͨ����������˿��ӫ���������ؼ�¼��ϸ����̬�ı仯��ֵ��ע����ǣ�����SMAD6��siRNA���Ŵ�����ANXA10-KOϸ���ָ�����������̬����PKD1������ʱҲ�۲쵽���Ƶı��ͣ�����SMAD6�µ���һ�������ʽ��ͬ����PKD1�Ĺ������SMAD6��siRNA���Ŷ���ǿ��ANXA10-KOϸ���Ķ���Ǩ�ơ���ANXA10-KOϸ�����ƣ�PKD1-KOϸ����Ǩ�Ƽ��٣�����ͨ��SMAD6��siRNA���Żָ���ͨ��transwell��Ϯʵ�飬����֤ʵ��B16F10ϸ������Ϯ�����ܵ�SMAD6����ˮƽ�����е��ء�SMAD6�Ĺ�������Ч��������ϸ����Ϯ����SMAD6����ˮƽ�ߵ�ANXA10-KOϸ���й۲쵽����ͬ�ı��͡��෴��siRNA���Ž鵼��SMAD6�ı������ƻָ���ANXA10-KOϸ������Ϯ��������Щ���������ANXA10ͨ��PKD1-SMAD6ͨ·�����˺�ɫ����ϸ��Ǩ�ơ�

8��ANXA10-PKD1-SMAD6�ں�ɫ�����еı��P���ٴ�����
Ϊ��ȷ��ANXA10��SMAD6�ں�ɫ����ת���е��ٴ����壬����ʹ��Oncomine™��Xu��ɫ�������ݼ�(����50��ԭ����ת��dz���Ժ�ɫ�����������������Ļ����������)����������Ϣѧ�������������DZ���֮�������ԡ������������������ɫ�����У�ANXA10��SMAD6�ı���ˮƽ�ʸ���ء����⣬ANXA10�ı����ϵ���SMAD6�ı����µ����ɫ����ת����ء�ͨ���Ի��ߺ�ɫ������֯���������黯Ⱦɫ����һ����֤����Щ����ģʽ�����ݻ��ߵ��ٴ�������������36������������Ϊ��ԭ���Ժ�ɫ����(n=24)��ת���Ժ�ɫ����(n=12)���顣�����黯����֤ʵ����ԭ����ɫ������ȣ�ת���Ժ�ɫ�������ֳ��ϸߵ�ANXA10����ϵ͵�SMAD6������⣬�����۲쵽PKD1��ANXA10�ı�������һ�£���ת���Ժ�ɫ�����б�ԭ����ɫ�����б�����ߡ���ˣ����ߵ����ݱ�����ANXA10-PKD1-SMAD6�ı���ģʽ���ٴ������ɫ����ת���йء�

�����
���ߵĽ��������ANXA10�ں�ɫ�����б����ϵ������ɫ�����Ľ�չ��ء������ϣ�ANXA10ͨ����PKD1��ϲ�����������TRIM41�鵼�ķ��ػ����ã������ϵ�PKD1�ĵ���ˮƽ��PKD1�ı����ϵ�������SMAD6�ı��SMAD6���µ��ٽ���E-cadherin��N-cadherin��ת������������˺�ɫ������ת�������� �ڱ��о��У�����ȷ��TRIM41��һ�����Խ���PKD1��E3��������ø����ANXA10��һ���µ�PKD1��ص��ף�������ǿPKD1���ȶ��ԡ���ΪPKD1����ˮƽ�ĵ������ӣ�ANXA10��TRIM41������PKD1�����ɫ�������Ʋ�����������ĺ�ѡҩ�ANXA10ͨ��PKD1�CSMAD6����;���ٽ���ɫ����ת�ơ�ANXA10-PKD1-SMAD6����ģʽ���ٴ������ɫ����ת����ء���ˣ���ANXA10-PKD1-SMAD6����о��������ڿ����µĺ�ɫ����ת�ư������Ʒ�����
�����
Zhang, Xuerui, et al. "ANXA10 promotes melanoma metastasis by suppressing E3 ligase TRIM41-directed PKD1 degradation." Cancer Letters (2021).





