ИЮЯИАћАЉ(Hepatocellular carcinoma, HCC)ЪЧИЮАЉЕФжївЊРраЭЃЌвбБЛжЄЪЕЮЊШЋЧђЕкЖўДѓАЉжЂЫРЭідвђЃЌЧвЗЂВЁТЪГЪЩЯЩ§ЧїЪЦЁЃЖдHCCМВВЁЗЂеЙЕФЧБдкЗжзгЛњжЦЕФШЯЪЖВЛзувдМАвђДЫЖјШБЗІгааЇЕФжЮСЦЪЧHCCдЄКѓВЛСМЕФжївЊдвђЁЃОЁЙмИЮАЉУтвпМьВщЕувжжЦМСЕФСйДВЪдбщНјеЙКмКУЃЌЕЋЫїРЗЧФсКЭРжЗЅЬцФсШдШЛЪЧФПЧАНігаЕФСНжжжЮСЦЭэЦкИЮАЉЕФвЛЯпбЁдёЁЃвђДЫЃЌМјЖЈИЮЯИАћАЉЕФЙІФмЕїПивђзгКЭжЮСЦАаЕуЃЌЖдПЊЗЂгааЇЁЂаТгБЕФПЙИЮЯИАћАЉжЮСЦЗНЗЈОпгаживЊвтвхЁЃ
бЁдёадМєНг(Alternative splicing, AS)ЪЧДѓЖрЪ§ецКЫЩњЮяЛљвђЖМЛсЩцМАЕФвЛжжзЊТМКѓЕїПиЙ§ГЬЁЃВЛЭЌЕФmRNAМєНгвьЙЙЬхБрТыВЛЭЌНсЙЙЛђЙІФмЕФЕААзжЪбЧаЭЃЌДгЖјЪЙЯИАћЕФЕААзжЪзщЖрбљЛЏЁЃЖјдкжзСіЯИАћжаЃЌе§ГЃЕФПЩБфМєНгЕїПиБЛШХТвЃЌДгЖјЕМжТСЫжзСіЬивьадRNAзЊТМЦзЃЌНјЖјДйНјСЫжзСіЯИАћЕФдіжГЁЂЧЈвЦЛђЬгвнЯИАћЫРЭіЁЃзюНќЖдЖржжЪЕЬхСіЕФДѓЙцФЃбаОПБэУїЃЌетаЉжзСіЬивьадМєНгФЃЪНгыМєНгвђзгЕФЪЇЕїгаЙиЃЌАќРЈМєНгЕїПиЛљвђЕФЭЛБфЁЂПНБДЪ§БфвьЛђБэДяИФБфЁЃетаЉЗЂЯжЪЙбаОПепЖджзСіЗЂеЙжаЕФМєНгвђзгЕФЪЇЕїдНРДдНИааЫШЄЃЌжМдкЮЊАЉжЂжЮСЦЬсЙЉаТЕФжЮСЦВпТдЁЃ
вьГЃПЩБфМєНгдкИЮЯИАћАЉжавВКмГЃМћЃЌЧвгыИЮАЉЕФЬиеїгаЙиЁЃДЫЭтЃЌЖржжПЩБфМєНгЕїПивђзгвбБЛБЈЕРВЮгыСЫИЮАЉЕФНјеЙЃЌАќРЈЃКSRSF2ЁЂSRSF3ЁЂhnRNPA2ЁЂPTBP3ЕШЁЃhnRNPUЪЧвЛжжживЊЕФМєНгЕїНквђзгЃЌЪєгкКЫФкВЛОљвЛКЫЬЧКЫЕААз(hnRNP)МвзхЃЌЕЋЦфдкHCCжаЕФзїгУЩаВЛУїШЗЁЃ
баОПТЗЯп
баОПФкШн
1ЁЂhnRNPUдкHCCжаБэДяЩЯЕїЧвгыHCCЛМепЕФСйДВЗжЦкКЭдЄКѓЯрЙи
зїепЪзЯШЭЈЙ§HCCDBЃЈИЮАЉЛљвђБэДяЭМЦзЃЉЗжЮіСЫhnRNPUдкИЮАЉЛМепБъБОжа mRNAЕФБэДяЃЌАќРЈСЫ268Р§HCCзщжЏЁЂ243Р§АЉХдзщжЏЁЂ40Р§ИЮгВЛЏзщжЏКЭ6Р§е§ГЃИЮдрзщжЏЁЃгые§ГЃИЮдрзщжЏЯрБШЃЌИЮгВЛЏзщжЏжаhnRNPUБэДяЫЎЦНЩ§ИпЃЌHCCзщжЏжаЕФhnRNPUБэДяИќИпЁЃДЫЭтЃЌгыАЉХдзщжЏЯрБШЃЌHCCзщжЏжаhnRNPUЕФБэДяУїЯдЩ§ИпЃЌЭЌЪБЃЌhnRNPUдкАЉХдзщжЏжаБШе§ГЃИЮдрБэДяТдИпЁЃНгЯТРДЃЌзїепЖдАќКЌ58Р§ИЮАЉбљЦЗЕФзщжЏаОЦЌНјааУтвпзщЛЏ(IHC)ШОЩЋРДМьВтhnRNPUЕААзБэДяЫЎЦНЁЃНсЙћБэУїЃЌhnRNPUдкжзСізщжЏжаОпгаЧПКЫШОЩЋЃЌЖјдкХфЖдЕФАЉХдзщжЏжаОпгаНЯШѕЛђвѕадКЫШОЩЋЁЃhnRNPUШОЩЋЧПЖШЕФЖЈСПЗжЮіНјвЛВНЯдЪОЃЌhnRNPUдкжзСіжаЕФБэДяУїЯдИпгкАЉХдзщжЏЁЃДЫЭтЃЌhnRNPUИпБэДяЕФИЮАЉЛМепЃЌTNMЗжЦкИпЧвЭљЭљЩњДцЪБМфНЯЖЬЃЌетгыШЫРрЕААзжЪЪ§ОнПтЕФНсЙћвЛжТЁЃетаЉНсЙћБэУїЃЌhnRNPUЖдHCCгаЧБдкЕФдЄКѓМлжЕЁЃзлЩЯЫљЪіЃЌзїепжЄУїСЫhnRNPUЕФБэДяЩ§ИпПЩФмдкHCCЕФНјеЙжаЗЂЛгживЊзїгУЁЃ

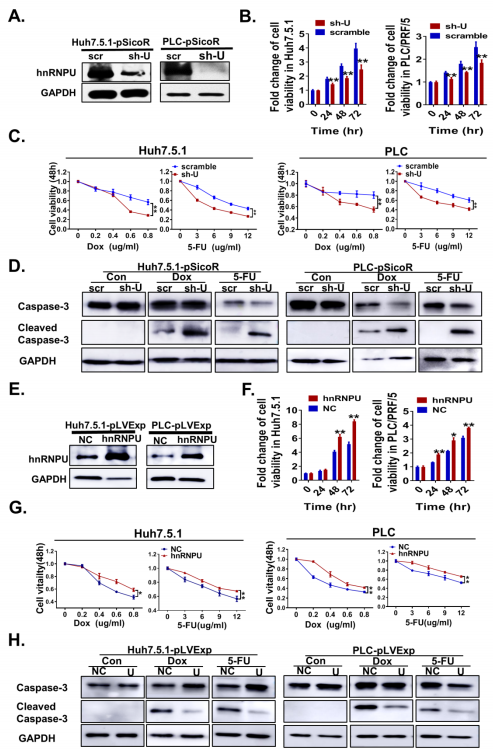
2ЁЂhnRNPUЕїПиИЮАЉЯИАћЕФдіжГЁЂФЭвЉКЭЛЏСЦгеЕМЕФЕђЭі
ЯИАћдіжГКЭЕђЭіЕФЪЇЕївЛжББЛШЯЮЊЪЧАЉЯИАћЕФЬиеїЃЌзїепНгЯТРДбаОПСЫhnRNPUЪЧЗёВЮгыСЫетаЉЙ§ГЬЕФЕїПиЁЃзїепНЈСЂСЫСНжъ hnRNPUЮШЖЈЧУГ§ЕФHCCЯИАћЯЕЃЌВЂЭЈЙ§western blot (WB)бщжЄСЫЧУГ§аЇЙћЁЃНсЙћБэУїЃЌhnRNPUЛљвђЧУГ§ЯджјМѕЛКСЫИЮАЉЯИАћЕФдіжГЃЌвВНЕЕЭСЫИЮАЉЯИАћЖдЛЏСЦвЉЮяАЂУЙЫи(Dox)КЭ5-ЗњФђрзрЄ(5-FU)ЕФФЭвЉадЁЃДЫЭтЃЌDoxЛђ5-FUПЩгеЕМЕђЭіБъжОЮяЃКМєНгЛюЛЏЕФcaspase-3дкИЮАЉЯИАћжаЗЂЩњЕЭБэДяЃЌЖјhnRNPUЕФЯТЕїПЩЕМжТМєНгЛюЛЏЕФcaspase-3ЕФНјвЛВНЛ§РлЃЌЬсЪОhnRNPUЕФЯТЕїМѕШѕСЫИЮАЉЯИАћЖдЛЏСЦЕФЕђЭіФЭвЉадЁЃдкhnRNPUЙ§БэДяЕФHCCЯИАћжавВЕУЕНСЫРрЫЦНсЙћЁЃНсЙћБэУїЃЌhnRNPUЕФЙ§БэДяПЩДйНјИЮАЉЯИАћЕФдіжГЁЂФЭвЉКЭЛЏСЦгеЕМЕФЕђЭіФЭвЉЁЃ
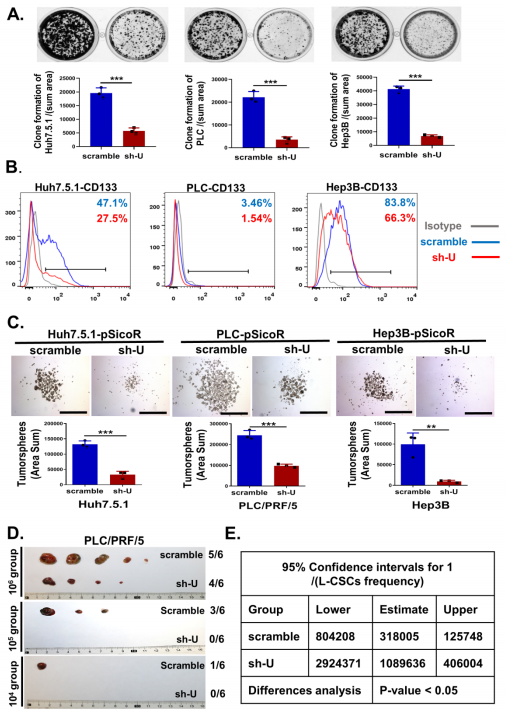
3ЁЂhnRNPUЕїПиИЮАЉЯИАћЕФздЮвИќаТКЭжТСіЧБФм
ИЮАЉЯИАћЕФздЮвИќаТЪЧжзСіЗЂЩњЗЂеЙЕФЙиМќЙ§ГЬЃЌзїепНјвЛВНбаОПСЫhnRNPUдкИЮАЉЯИАћздЮвИќаТжаЕФЕїПизїгУЁЃНсЙћБэУїЃЌгыscramblesЖдееЯрБШЃЌhnRNPUЕФЛљвђЧУГ§ЯджјНЕЕЭСЫИЮАЉЯИАћЕФМЏТфаЮГЩФмСІЁЃhnRNPUдкИЮАЉЯИАћжаЛљвђЧУГ§КѓЃЌИЮАЉИЩЯИАћБэУцБъжОЮяCD133БэДяЯТЕїЃЌЖјhnRNPUЕФЙ§БэДядђдіМгСЫИЮАЉЯИАћжаCD133ЕФБэДяТЪЁЃЭЈЙ§Ш§ЮЌжзСіЧђОлЬх(вЛжждкЬхЭтИЛМЏКЭЮЌГжИЩЯИАћбљЯИАћЕФЗНЗЈ)ЪЕбщЃЌзїепНјвЛВНжЄЪЕСЫhnRNPUдкИЮАЉЯИАћЕФжзСіЧђаЮГЩЧБФмЗНУцЗЂЛгСЫживЊзїгУЁЃетаЉНсЙћБэУїЃЌhnRNPUдкЬхЭтЕїПиИЮАЉЯИАћЕФздЮвИќаТЁЃДЫЭтЃЌдкгаЯоЯЁЪЭЪдбщжаЃЌзїепНЋ106/105/104ИіPLC-scrambleЯИАћКЭЯрЭЌЪ§СПЕФPLC-hnRNPUЧУГ§ЯИАћЗжБ№вЦжВЕНNOD/SCIDаЁЪѓЕФзѓгвВрЁЃ4жмКѓЃЌМЦЫужзСіЗЂЩњТЪЃЌгУELDAШэМўЗжЮіжзСіЦ№ЪМЯИАћЕФЦЕТЪЁЃscrambleзщКЭЧУЕЭзщЕФЦ№ЪМжзСіЯИАћЦЕТЪЗжБ№ЮЊ1/318005КЭ1/1089636ЃЌЬсЪОhnRNPUЕФЧУГ§ЯджјНЕЕЭСЫИЮАЉЯИАћЕФжТСіЧБФмЁЃетаЉНсЙћБэУїЃЌhnRNPUдкЬхЭтКЭЬхФкОљФмЕїПиИЮАЉЯИАћЕФздЮвИќаТЁЃ
4ЁЂc-MycдкзЊТМЫЎЦНЕїПиhnRNPUЖјhnRNPUЮЌГжc-MycЕФmRNAЮШЖЈ
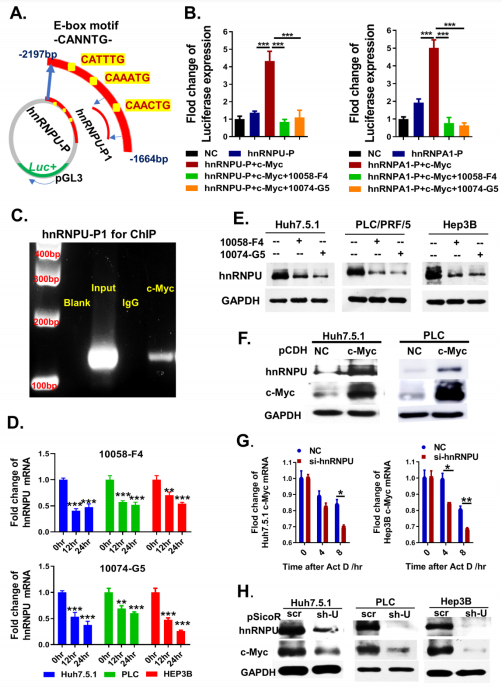
ЮЊСЫСЫНтhnRNPUдкHCCНјеЙжаЕФЩЯЕїдвђЃЌзїепЪзЯШЗжЮіСЫTCGA-LIHCбљБОжаhnRNPUЕФЛљвђБэДяЧщПіЃЌНсЙћБэУїЃЌжЛгаЩйЪ§ВЁР§hnRNPU mRNAЕФИпБэДяПЩФмгыЛљвђзщРЉдігаЙиЃЌЖјДѓЖрЪ§ВЁР§ВЛЯрЙиЁЃвђДЫЃЌзїепНгЯТРДДгhnRNPUЕФзЊТМЕїПижабАевжЄОнЁЃзїепдкhnRNPUЕФЦєЖЏзгЧјЗЂЯжСЫМИИіc-MycНсКЯЮЛЕуЃЈE-boxађСаЃЉЃЌЖјc-MycвбБЛЙуЗКжЄУїгыАЉжЂжаЕФМєНгЬхКЭвьГЃМєНгЯрЙиЁЃHNRNPA1ЁЂHNRNPA2ЁЂPTBЁЂSRSF1ЁЂPRMT5ЕШМєНгвђзгвбБЛжЄУїЮЊc-MycЕФжБНгзЊТМАаЕуЁЃвђЖјзїепЭЦВтЃЌhnRNPUПЩФмЪЧИЮАЉжаc-MycЕФвЛИіаТЕФЧБдкзЊТМАаЕуЁЃвђДЫЃЌзїепВЩгУЫЋгЋЙтЫиУИБЈИцЛљвђММЪѕРДМьВтc-MycЖдhnRNPUЕФзЊТМЕїПизїгУЁЃдкзЊШыpCDH-c-MycКѓЃЌhnRNPUЦєЖЏзг(-2197жС-1664bpЃЌАќКЌШ§ИіE-boxађСа)ЕФгЋЙтЫиУИЛюадЩЯЕїЃЌЖјc-MycвжжЦМС10058-F4КЭ10074-G5ЕФМгШыЪЙгЋЙтЫиУИЛюадНјЖјЯТЕїЁЃвбжЊЕФc-MycАаЛљвђЃКhnRNPA1ЕФЦєЖЏзгдкИУЪЕбщжазїЮЊбєадЖдееЁЃетаЉНсЙћБэУїЃЌc-MycПЩФмдкЕїПиhnRNPUзЊТМЗНУцЗЂЛгзХЛ§МЋЕФзїгУЁЃзїепЭЈЙ§ШОЩЋжЪУтвпГСЕэ(ChIP)ЪЕбщЃЌжЄЪЕСЫc-MycПЩвдгыhnRNPUЕФЦєЖЏзгЧјгђНсКЯЁЃДЫЭтЃЌc-MycЕФвжжЦМСдкmRNAЫЎЦНКЭЕААзЫЎЦНОљПЩвдЯТЕїhnRNPUЕФБэДяЃЌЖјc-MycЕФЙ§БэДяДйНјСЫhnRNPUЕФБэДяЁЃвдЩЯНсЙћБэУїЃЌc-MycдкHCCЯИАћжаЪЧhnRNPUЕФе§ЯђзЊТМЕїПивђзгЁЃ
ДЫЭтЃЌгаБЈЕРГЦhnRNPUЭЈЙ§гыIGF2BP1вдRNAвРРЕЕФЗНЪННсКЯЮШЖЈc-MYCЕФmRNAЃЌзїепНгЯТРДМьВтСЫhnRNPUЪЧЗёдкHCCЯИАћжаЕїПиc-MYC mRNAЕФЮШЖЈадЁЃзїепНЋhnRNPUЕФБэДяЧУГ§ЃЌВЂдкЗХЯпОњЫиDЃЈвЛжжзЊТМвжжЦМСЃЉДІРэКѓЃЌдкжИЖЈЪБМфВтСПc-MYC mRNAЕФБэДяЫЎЦНЁЃНсЙћЯдЪОЃЌдкhnRNPUЛљвђЧУГ§ЕФHep3BЯИАћжаЃЌc-MYCЕФmRNAдкЗХЯпОњЫиDДІРэ4аЁЪБКѓБэДяЯТЕїЫйЖШПьгкhnRNPU-normal Hep3BЯИАћЃЛЖјЗХЯпОњЫиDДІРэ8аЁЪБКѓЃЌhnRNPUЛљвђЧУГ§ЕФИЮАЉЯИАћжаc-MYCЕФmRNAБэДяЯТНЕЫйЖШУїЯдИпгкЖдеезщЁЃЯргІЕиЃЌдкhnRNPUЛљвђЧУГ§ЕФHCCЯИАћжаЃЌc-MycЕААзБэДяЫЎЦННЕЕЭЃЌЖјдкhnRNPUЛљвђЙ§БэДяЕФHCCЯИАћжаЃЌc-MycЕААзЫЎЦНЩ§ИпЁЃетаЉНсЙћЬсЪОЃЌhnRNPUПЩЮШЖЈc-MYCЕФmRNAЃЌЕїНкЦфЕААзБэДяЁЃ
5ЁЂhnRNPUгыc-MycдкHCCбљБОжаЕФБэДяГЪе§ЯрЙи
ЖдTCGA-LIHCЪ§ОнМЏжаЕФСйДВHCCЛМепЪ§ОнЗжЮіБэУїЃЌc-MycгыhnRNPUдкmRNAЕФБэДяЫЎЦНГЪе§ЯрЙиЁЃзїепдк15Р§дЗЂадHCCбљБОжаМьВтЃЌНсЙћБэУїЃЌЖўепЕФЕААзЫЎЦНвВГЪе§ЯрЙиЁЃгаШЄЕФЪЧЃЌзїепЗЂЯждк2КХЛМепАЉХдзщжЏЕФвѕадШОЩЋБГОАжаЗЂЯжСЫc-MycКЭhnRNPUЙ§БэДяЕФЮЂзЊвЦдюЁЃетвЛЗЂЯжНјвЛВНжЄЪЕСЫетСНжжЕААздкHCCжаЕФУмЧаЯрЙиадЁЃ

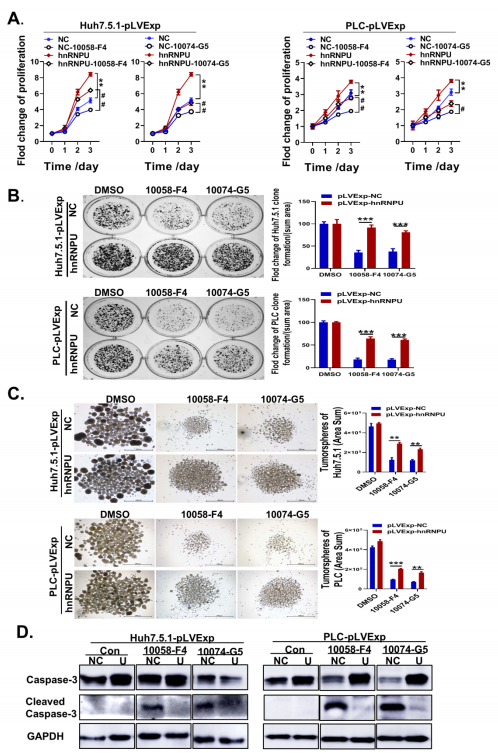
6ЁЂhnRNPUЙ§БэДяПЩВПЗжЯћГ§ИЮАЉЯИАћжаc-MycвжжЦМСЕФзїгУ
c-MycЪЧвЛжжЧПжТАЉЛљвђЃЌЭЈЙ§ЕїНквЛаЉЯТгЮаХКХЭЈТЗРДЮЌГжАЉЯИАћЕФЩњДцКЭздЮвИќаТЃЌЖјЧвc-MycКЭhnRNPUжЎМфДцдкЯрЛЅЕїПиЁЃзїепНгЯТРДбаОПСЫhnRNPUдкИЮАЉЯИАћжаc- mycНщЕМЕФЩњЮябЇЙ§ГЬжаАчбнЪВУДНЧЩЋЁЃзїепЪЙгУc-MycвжжЦМСзшЖЯСЫc-MycНщЕМЕФЩњЮябЇЙІФмЃЌВЂМьВтСЫhnRNPUЙ§БэДяЖдc-MycЙІФмвжжЦЕФгАЯьЁЃдкИЮАЉЯИАћжав§ШыЭтдДадhnRNPUЃЌзїепЗЂЯжЃЌhnRNPUЕФЙ§БэДяВПЗжЯћГ§СЫ10058-F4КЭ10074-G5ЕФЩњГЄвжжЦзїгУЁЃhnRNPUЙ§БэДяЯИАћЕФМЏТфаЮГЩФмСІвВЖдc-MycвжжЦМСБэЯжГіИќИпЕФФЭвЉадЁЃДЫЭтЃЌ10058-F4Лђ10074-G5ЯджјНЕЕЭСЫжзСіЧђЕФЪ§СПКЭЬхЛ§ЃЌЖјhnRNPUЕФЙ§БэДяВПЗжФцзЊСЫетСНжжc-MycвжжЦМСЫљв§Ц№ЕФздЮвИќаТвжжЦЁЃВЛНіШчДЫЃЌдк10058-F4Лђ10074-G5ДІРэЕФИЮАЉЯИАћжаЃЌдк48аЁЪБФкПЩгеЕММєЧаЛюЛЏЕФcaspase-3БэДяЃЌЖјhnRNPUЙ§БэДяПЩвжжЦМєЧаЛюЛЏcaspase-3ЕФгеЕМЃЌЫЕУїhnRNPUЕФЙ§БэДяПЩКмДѓГЬЖШЭьОШc-MycвжжЦМСгеЕМЕФИЮАЉЯИАћЕђЭіЁЃ
ЩЯЪіНсЙћБэУїЃЌhnRNPUдкИЮАЉЯИАћжаЙ§БэДяПЩВПЗжЛжИДc-MycвжжЦМСЕФдіжГЁЂздЮвИќаТвжжЦзїгУКЭгеЕМЕђЭізїгУЃЌЬсЪОhnRNPUдкc-MycНщЕМЕФИЮАЉЯИАћЩњЮябЇЙ§ГЬжаЗЂЛгживЊзїгУЁЃ
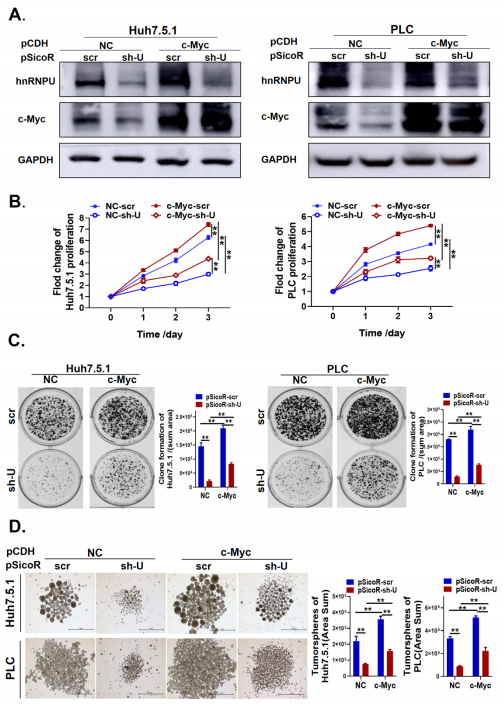
7ЁЂc-MycЕФЙ§БэДяПЩВПЗжФцзЊИЮАЉЯИАћжаhnRNPUЛљвђЧУГ§ЕФгАЯь
МШШЛhnRNPUдкИЮАЉЯИАћжаВЮгыСЫc-MycНщЕМЕФЩњЮябЇзїгУЃЌc-MycЪЧЗёвВЛсгАЯьhnRNPUдкИЮАЉЯИАћжаЕФЩњЮябЇзїгУФи?зїепНгЯТРДЬНЬжСЫc-MycЕФЙ§БэДяЖдhnRNPUЧУГ§ЕФИЮАЉЯИАћЩњЮябЇЙІФмЕФгАЯьЁЃНЋc-MycЙ§БэДядиЬх(pCDH-RFP-c-Myc)ЁЂhnRNPUЧУГ§диЬх(pScioR-GFP-sh-hnRNPU)МАЯргІЕФЖдеедиЬх(pCDH-RFP-NC/ pScioR-GFP-scramble)зЊШОШыИЮАЉЯИАћЃЌСїЪНЯИАћММЪѕЖдзЊШОЕФЯИАћИЛМЏЃЌВЂНјааwestern blotбщжЄЁЃНсЙћБэУїЃЌc-MycЕФЙ§БэДявВФмВПЗжФцзЊhnRNPUЛљвђЯТЕїЖдЯИАћдіжГЁЂМЏТфаЮГЩКЭжзСіЧђаЮГЩЕФвжжЦзїгУЁЃНсЙћжЄУїСЫc-MycВПЗжВЮгыСЫhnRNPUНщЕМЕФHCCЯИАћЕФЩњЮябЇЙІФмЁЃ
баОПНсТл
зїепЗЂЯжhnRNPUдкHCCзщжЏжаИпБэДяЃЌЧвгыHCCЛМепЕФдЄКѓВЛСМгаЙиЁЃДЫЭтЃЌhnRNPUдкЕїПиИЮАЉЯИАћЕФдіжГЁЂЕђЭіЁЂздЮвИќаТКЭжТСіЧБФмЗНУцОпгаживЊвтвхЁЃЛњжЦЩЯЃЌc-MycдкзЊТМЫЎЦНЕїПиhnRNPUЕФБэДяЃЌЭЌЪБhnRNPUЮШЖЈc-MycЕФmRNAЁЃзїепЗЂЯжhnRNPUКЭc-MycЕїПиЛЗЖдИЮАЉЕФдіжГКЭздЮвИќаТОпгааЭЌзїгУЃЌВЂДйНјИЮАЉЕФНјеЙЁЃзлЩЯЫљЪіЃЌhnRNPUзїЮЊвЛИіаТЕФc-MycзЊТМАаЕуЃЌДйНјИЮАЉЕФНјеЙЃЌетПЩФмГЩЮЊжЮСЦc-MycЧ§ЖЏЕФИЮАЉЕФвЛИігаЧАЭОЕФАаЕуЁЃ
ВЮПМЮФЯз
Zhang B, Wang H Y, Zhao D X, et al. hnRNPU Functions as a Novel Therapeutic Target of c-Myc in the Progression of Hepatocellular Carcinoma[J]. FEBS Letters, 2020.





